近日,甘李药业(603087)自主研发的1类新药—博凡格鲁肽(GZR18)注射液,在中国超重/肥胖患者中完成的Ib/IIa期临床研究结果正式发表于国际权威期刊《Cell Reports Medicine》。作为Cell Press旗下的旗舰级医学期刊,其2025年影响因子达10.6,位列中科院分区医学大类1区(Top期刊),是生物医学领域备受认可的高影响力学术期刊。该研究结果表明:博凡格鲁肽注射液可以显著降低体重、同时改善多项心血管和代谢危险因素,且总体安全性和耐受性良好。

图片来源:《Cell Reports Medicine》
研究设计
该研究是一项随机、双盲、安慰剂对照的Ib/IIa期多次递增剂量临床试验,在中国4个研究中心共入组60例中国超重/肥胖成人患者。本研究包含两个部分: A部分:24例超重/肥胖受试者随机接受每周一次博凡格鲁肽注射液(目标剂量4.8 mg,剂量递增方案:0.6-1.2-2.4-3.0-3.6-4.2-4.8 mg)或安慰剂,治疗周期(883436)为26周(含12周剂量维持期);B部分:36例肥胖受试者随机接受每周一次博凡格鲁肽注射液(目标剂量30 mg,剂量递增方案:1.5-3-5-7-9-12-15-18-24-30 mg)或安慰剂,治疗周期(883436)为35周。自9 mg剂量起,B部分还探索了博凡格鲁肽注射液每两周一次的给药频率。研究的主要终点为博凡格鲁肽注射液在受试者中的安全性和耐受性,以及治疗结束时体重较基线变化的百分比。
研究结果
研究结果显示,博凡格鲁肽注射液可显著降低体重,主要结果如下:
A部分:
治疗26周后,博凡格鲁肽组体重较基线变化百分比为-9.36%,安慰剂组为6.68%,组间差值达-16.1% (95% CI: -26.4, -5.7);
博凡格鲁肽组中66.7%的受试者实现体重降幅≥5%,而安慰剂组无受试者达到该标准。

图2-博凡格鲁肽对比安慰剂的体重变化情况 (A部分)
A) 体重较基线变化百分比折线图;B) 26周时体重降幅≥5%的受试者比例。
基于全分析(FAS),采用协方差分析(ANCOVA)模型,图A数据以最小二乘均值(LSM)±标准误(SE)表示。图B展示第26周时体重达标的受试者比例(FAS中达标人数除以总人数)。样本量:GZR18 4.8 mg每周一次(QW)组: n=18; 安慰剂组(Placebo): n=6。
B部分:
治疗35周后,博凡格鲁肽注射液每周一次(QW)组体重较基线变化百分比为-17.8%, 每两周一次(Q2W)组为-12.8%,安慰剂组为0.7%,两组较安慰剂的差值分别为-18.6% (95% CI: -25.5, -11.6)和-13.5% (95% CI: -21.0, -6.0);且35周时接受博凡格鲁肽治疗的受试者体重下降趋势尚未到达平台期;
QW组中,体重降幅≥5%、10%、15%和20%的受试者比例分别为100%,90%,80%和40%; Q2W组中相应比例为71.4%,71.4%,42.9%和14.3%;而安慰剂组无受试者实现体重降幅≥5%。
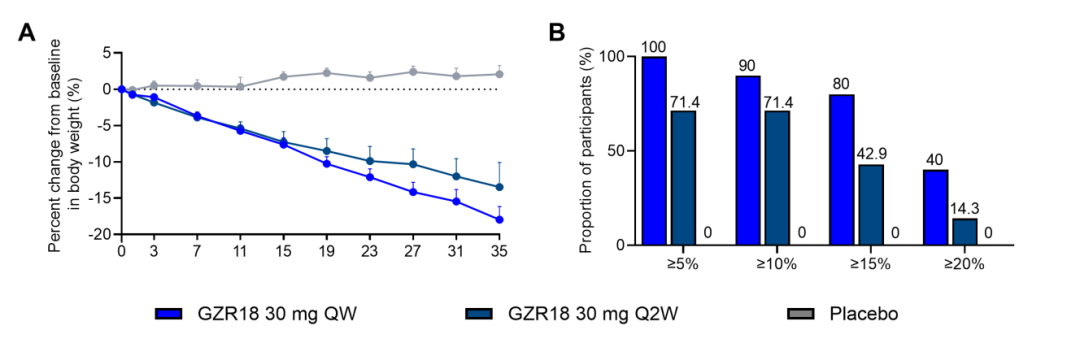
图3-博凡格鲁肽对比安慰剂的体重变化情况 (B部分)
A) 体重较基线变化百分比折线图;B) 35周时体重降幅≥5%, 10%, 15%和20%的受试者比例。
基于FAS,采用ANCOVA模型,图A数据以LSM±SE表示;样本量:GZR18 30 mg每周一次(QW)组: n=16; GZR18 30 mg每两周一次(Q2W)组: n=10; 安慰剂组(Placebo): n=9 。图B展示第35周时体重达标的受试者比例(FAS中达标人数除以完成第35周体重测量的受试者人数);样本量:GZR18 30 mg每周一次(QW)组: n=10; GZR18 30 mg每两周一次(Q2W)组: n=7; 安慰剂组(Placebo): n=5。
此外,博凡格鲁肽治疗还改善了多项心血管和代谢危险因素,包括腰围、血糖、血压、血脂和肝酶水平等,其中在B部分中的改善尤为显著。
博凡格鲁肽总体安全性和耐受性良好,未见与药物相关的严重不良事件;其安全性特征与其他GLP-1RA类药物一致,主要表现为轻至中度胃肠道不良反应。
本研究结果首次提示了博凡格鲁肽注射液每两周一次给药方案的可行性,治疗35周后体重降幅达12.8%且安全性、耐受性良好,为其开发 “两周一次”的给药方案提供了有力依据。甘李药业(603087)已完成的博凡格鲁肽的IIb期减重临床研究,进一步评估了更高剂量及“两周一次“给药方案的疗效和安全性。该研究结果已于2026年2月27日发表于Nature出版社顶刊《Signal Transduction and Targeted Therapy》(IF:52.7)。
关于博凡格鲁肽
甘李药业(603087)自主研发的博凡格鲁肽(研发代号:GZR18)注射液是一种每两周给药一次的GLP-1RA,旨在治疗肥胖/超重及2型糖尿病。临床研究数据显示博凡格鲁肽能有效减轻体重和降低血糖,并综合改善其他代谢相关指标,而且其安全性和耐受性特征与GLP-1RA类药物一致,有望成为全球首款上市的GLP-1RA双周制剂。目前,博凡格鲁肽注射液的全球开发已进入III期临床研究阶段。
